Accueil Dossiers Les armes secrètes du biofilm
Les armes secrètes du biofilm
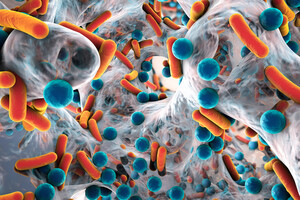
Le système immunitaire est programmé pour neutraliser et, si possible, détruire tout micro-organisme qu’il reconnaît comme étranger. Mais le biofilm rend le système immunitaire inopérant en s’oppose à la pénétration des traitements dans les bactéries. Zoom sur les armes secrètes du biofilm pour aider les bactéries à proliférer
Il permet à celles-ci de modifier leur métabolisme et d’échapper ainsi au mode d’action des antibiotiques. Les gènes de résistance développés par certaines bactéries sont transférés aux autres membres de la même communauté. S’il y parvient le plus souvent facilement lorsque l’agent infectieux est de forme planctonique (non organisé en colonie), il est régulièrement mis en échec lorsque l’agent infectieux se protège derrière un biofilm.
Les armes secrètes du biofilm
Notre système immunitaire ne reste pas pour autant inactif ou paralysé par le biofilm. En effet, il continue à entretenir un terrain inflammatoire tout autour, ce qui non seulement est vain, mais permet aux micro-organismes retranchés dans leur matrice protectrice d’augmenter leurs ressources en nutriments indispensables à leur métabolisme, à leur régénération et à leur multiplication !
Le biofilm est une barrière presque infranchissable : lorsqu’il parvient à maturité, les micro-organismes qui ont travaillé de concert à sa constitution ne représentent plus que 20 % de son volume. En milieu liquide, il lui suffit de 24 à 48 heures pour atteindre le stade de la maturité. Par ailleurs, une partie des micro-organismes rassemblés au cœur du biofilm retourne à l’état planctonique, parfois sous l’effet des contraintes environnementales, parfois de façon programmée : la création d’autres biofilms à plus ou moins grande distance garantit la pérennité des souches envahisseuses chez son hôte.
Ces emboles septiques peuvent alors gagner n’importe quel organe et provoquer des épisodes infectieux dramatiques, voire mortels, particulièrement ...
Cet article est réservé à nos abonnés. Vous êtes abonnés ? Connectez-vous
Pourquoi cet article est réservé aux abonnés ?
Depuis maintenant près de 30 ans, Alternative Santé promeut les bienfaits des médecines douces ou des approches complémentaires.
Alors qu'elle sont attaquées de toute part avec la plus grande virulence, notre missions est plus que jamais essentielle pour défendre une autre vision de la santé.
C'est pourquoi nous avons besoin de vous pour nous soutenir dans nos actions d'information. En effet, si nous souhaitons garder notre indépendance éditoriale, seul votre soutien financier peut nous permettre de continuer notre mission :
- celle de dénoncer les scandales et dérives inquiétantes dans le monde de la santé, de mettre en lumière les effets indésirables
- celle de faire connaitre les solutions préventives et les remèdes naturels efficaces au plus grand nombre
- celle de défendre le droit des malades, des usagers de santé et des médecins à choisir librement les meilleurs remèdes.
Comme vous le savez certainement, nous ne mettons aucune publicité dans notre journal et restons libres de toute pression. Nous souhaitons garder toute notre indépendance, mais cette liberté a un coût.
La meilleure façon de nous aider et de soutenir une presse indépendante est donc de vous abonner à notre journal !
Je m'abonne
En aucun cas les informations et conseils proposés sur le site Alternative Santé ne sont susceptibles de se substituer à une consultation ou un diagnostic formulé par un médecin ou un professionnel de santé, seuls en mesure d’évaluer adéquatement votre état de santé


 Découvrir le numéro
Découvrir le numéro  "En milieu liquide il suffit de 24 à 48h pour que le biofilm atteigne sa maturité"
"En milieu liquide il suffit de 24 à 48h pour que le biofilm atteigne sa maturité"



La médecine officielle en difficulté
L'hygiène préventive contre les biofilms
Les biofilms : nouvelle frontière de la lutte antibactérienne
Remèdes naturels anti-biofilms