Accueil Dossiers Auto-anticorps, antigène, l’intolérance de soi
Auto-anticorps, antigène, l’intolérance de soi
Depuis quelques décennies, les maladies auto-immunes (MAI) font aussi peur que le cancer ou les maladies cardiovasculaires. Et pour cause, elles sont la troisième cause de mortalité sous nos latitudes. Causées par un dysfonctionnement du système immunitaire, elles ne doivent pas pour autant être confondues avec les maladies auto-inflammatoires. Quels sont les traitements actuels pour les personnes atteintes, et quels conseils supplémentaires leur donner en matière de nutrition et approches complémentaires ? (Dossier partie II)
La fonction du système immunitaire est de reconnaître et d’éliminer tout élément étranger à l’organisme dont il participe. Dans la genèse des MAI, c’est une perturbation du fonctionnement des lymphocytes B et T qui est en cause.
Normalement, alors que la plupart des lymphocytes B et T sont programmés pour reconnaître les antigènes portés par les agents pathogènes, d’autres populations de lymphocytes B et T développent des anticorps contre les antigènes présents sur les organes (autoanticorps) : en effet, sous l’effet du vieillissement physiologique, les gènes s’altèrent peu à peu et les protéines dont ils contrôlent la synthèse ne présentent plus tout à fait la composition et la forme spatiale des premiers instants de la vie, de sorte qu’elles sont considérées comme des substances étrangères par le système immunitaire. Fort heureusement, ces autoanticorps sont détruits dans leur grande majorité au niveau du thymus et de la moelle osseuse, puis ceux qui ont échappé à cette première traque sont finalement éliminés par un processus périphérique. Du fait de cette tolérance immunologique, c’est le temps béni de l’auto-immunité physiologique.
Puis, suite à un concours particulier de circonstances, ces cellules perdent leur pouvoir discriminatoire et ne font donc plus la différence entre agents pathogènes et organisme. Du fait de la rupture de la tolérance immunologique, c’est alors le temps de l’auto-immunité pathologique et la venue d’une ou plusieurs MAI.
Ainsi, se développe un terrain inflammatoire chronique, alimenté le plus ...
Cet article est réservé à nos abonnés. Vous êtes abonnés ? Connectez-vous
Pourquoi cet article est réservé aux abonnés ?
Depuis maintenant près de 30 ans, Alternative Santé promeut les bienfaits des médecines douces ou des approches complémentaires.
Alors qu'elle sont attaquées de toute part avec la plus grande virulence, notre missions est plus que jamais essentielle pour défendre une autre vision de la santé.
C'est pourquoi nous avons besoin de vous pour nous soutenir dans nos actions d'information. En effet, si nous souhaitons garder notre indépendance éditoriale, seul votre soutien financier peut nous permettre de continuer notre mission :
- celle de dénoncer les scandales et dérives inquiétantes dans le monde de la santé, de mettre en lumière les effets indésirables
- celle de faire connaitre les solutions préventives et les remèdes naturels efficaces au plus grand nombre
- celle de défendre le droit des malades, des usagers de santé et des médecins à choisir librement les meilleurs remèdes.
Comme vous le savez certainement, nous ne mettons aucune publicité dans notre journal et restons libres de toute pression. Nous souhaitons garder toute notre indépendance, mais cette liberté a un coût.
La meilleure façon de nous aider et de soutenir une presse indépendante est donc de vous abonner à notre journal !
Je m'abonne
En aucun cas les informations et conseils proposés sur le site Alternative Santé ne sont susceptibles de se substituer à une consultation ou un diagnostic formulé par un médecin ou un professionnel de santé, seuls en mesure d’évaluer adéquatement votre état de santé
Des causes souvent inconnues, une recherche qui avance…
Maladies auto-immunes : du diagnostic au traitement en médecine officielle
Maladies auto-immunes : l'apport des médecines naturelles

Vivre avec une maladie auto-immune : soins allopathiques et appproches naturelles

Maladies auto-immunes : les conseils en nutrition, micronutrition et phytothérapie



 Découvrir le numéro
Découvrir le numéro 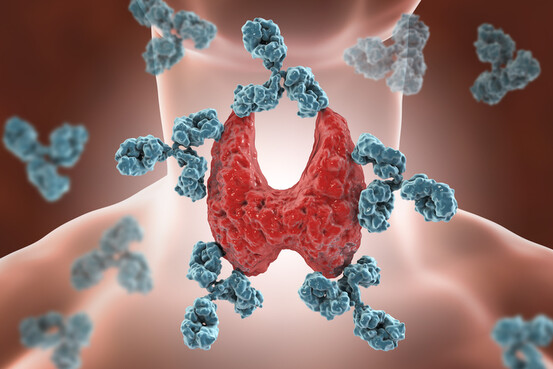 Lors d'une maladie d'Hashimoto, les anticorps s'attaquent à la thyroïde
Lors d'une maladie d'Hashimoto, les anticorps s'attaquent à la thyroïde
Des causes souvent inconnues, une recherche qui avance…
Maladies auto-immunes : du diagnostic au traitement en médecine officielle
Maladies auto-immunes : l'apport des médecines naturelles
Vivre avec une maladie auto-immune : soins allopathiques et appproches naturelles
Maladies auto-immunes : les conseils en nutrition, micronutrition et phytothérapie